98. Methanol und Ethanol - Bedeutung
Vielseitige Verwendbarkeit der beiden Alkohole
Wegen ihrer in chemischer Hinsicht großen Ähnlichkeit kann man Methanol und Ethanol für gleiche Zwecke verwenden. Beide kann man als Lösungsmittelfür Lacke und Firnisse, für Fette, Öle und Harze einsetzen. Auch als Frostschutzmittel finden beide Verwendung.

Beide Alkohole kann man als Energieträger nutzen. Ethanol findet als Brennspiritus und Benzinzusatz (z.B. Bioethanol in E10) Verwendung. Methanol wird unter anderem als Ausgangsmaterial in der chemischen Industrie oder ebenfalls als Energielieferant genutzt. In Brennstoffzellen dient Methanol als Wasserstofflieferant. Die Verwendung als Kraftstoff, so genanntes Fuel-Methanol, wird intensiv untersucht. Möglich ist der Zusatz zu herkömmlichen Motorkraftstoffen oder die Verwendung reinen Methanols, wobei die Schwefelfreiheit eine saubere Verbrennung erlaubt.
Bei der Synthese vieler Stoffe stellen beide Alkohole wichtige Zwischenprodukte dar. Ethanol ist ein wichtiges Lösungsmittel und Zwischenprodukt in der Chemischen Industrie. Ein wichtigstes Folgeprodukt ist Ethylchlorid, das aus Ethanol durch Umsetzung mit Chlorwasserstoff hergestellt wird. Die Oxidation liefert weitere Folgeprodukte wie Acetaldehyd und Essigsäure.
Ethanol wird in einer Vielzahl von Veresterungsreaktionen eingesetzt. Die erhaltenen Ester (Kapitel 106) haben vielfältige Verwendungsmöglichkeiten als Lösungsmittel und als Zwischenprodukt für Folgesynthesen. Ein wichtiges Folgeprodukt ist Ethylacrylat, ein Monomer, das als Co-Monomer in verschiedenen Polymerisationsprozessen eingesetzt wird. Essigsäureethylester wird als Lösungsmittel für Klebstoffe und Nagellack und zur Extraktion von Antibiotika eingesetzt. Glycolether wie 2-Ethoxyethanol sind als Lösungsmittel für Öle, Harze, Fette, Wachse, Nitrozellulose und Lacke weit verbreitet.
Ethanol findet Verwendung in den drei Hauptmärkten Alkoholische Getränke, als Rohstoff für die chemische Industrie und als Energieträger. Ethanol, das aus der Vergärung von Zucker- und stärkehaltigen Lebensmitteln stammt, wird in allen Bereichen eingesetzt, während synthetisches Ethanol nur als Chemierohstoff und Energieträger verwendet wird.
Die Hauptmenge des produzierten Ethanols wird in Form von alkoholischen Getränken für Genusszwecke verbraucht. Es dient weiterhin als Lösungsmittel sowohl für Konsumprodukte unter anderem im Haushalt (Parfüm, Deodorant), als auch für medizinische Anwendungen (Lösungsmittel für Medikamente, Desinfektionsmittel) sowie in der Industrie selbst ebenfalls als Lösungsmittel und allgemein als Brennstoff.
Methanol und Ethanol kann man leicht unterscheiden
Manchmal ist es wichtig, Methanol und Ethanol zu unterscheiden. Möglich macht dies die Reaktion beider Alkohole mit Borsäure. Mit Methanol und Borsäure entsteht eine Verbindung, die sofort mit grüner Flamme brennt. Die Verbrennung beim Ethanol erfolgt erst nach geraumer Zeit mit grüner Flamme (Versuch 1).
Herstellung
Metanol
Dem Chemiker Matthias Pier gelang 1923 die großtechnische Herstellung von Methanol aus Synthesegas im Hochdruckverfahren an Zinkoxid-Chromoxid-Katalysatoren.
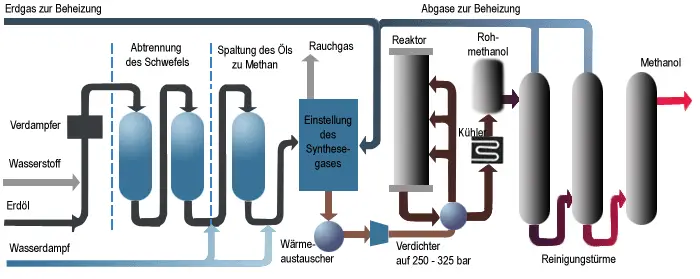
Bis zu diesem Zeitpunkt wurde Methanol nur durch trockene Destillation von Holz gewonnen. Damit war neben Ammoniak ein weiteres Grundprodukt der industriellen Chemie durch Hochdruckverfahren zugänglich. Die Methanolherstellung lässt sich in die Schritte Synthesegasherstellung, Roh-Methanolherstellung und Aufarbeitung des Roh-Methanols unterteilen (siehe Schema unten). Das Synthesegas kann aus einer Reihe verschiedener fossiler und nachwachsender Rohstoffe wie Kohle, Braunkohle, schweren Erdölfraktionen, Müll, Torf, Holz, Biogas oder Klärschlamm gewonnen werden.
$ \mathrm {CO + 2 \ H_2 \ {\large \leftrightharpoons} \ CH_3OH + 90,8 \ kJ } $
Etanol
Ethanol kann sowohl über Ethin als auch Ethen erhalten werden. Nach wie vor wird ein erheblicher Teil des Ethanols durch Gärung aus Biomasse, meist aus Zucker- oder Stärke-haltigen Feldfrüchten oder traditionell aus Produkten des Gartenbaus gewonnen. Dieser Prozess wird mit einer Reihe von Nahrungsmitteln kontrolliert durchgeführt, wodurch zum BeispielWein aus Weintrauben oder Bier aus Malz und Hopfen entstehen.
$ \mathrm {C_6H_{12}O_6 \ \longrightarrow \ 2 \ C_2H_5OH + 2 \ CO_2 + 88 \ kJ} $