Homocystein
| Strukturformel | ||||||||
|---|---|---|---|---|---|---|---|---|
| Allgemeines | ||||||||
| Name | L-Homocystein | |||||||
| Andere Namen |
| |||||||
| Summenformel | C4H9NO2S | |||||||
| CAS-Nummer |
| |||||||
| Kurzbeschreibung |
farblose Kristalle[1] | |||||||
| Eigenschaften | ||||||||
| Molare Masse | 135,18 g·mol−1 | |||||||
| Aggregatzustand |
fest | |||||||
| Schmelzpunkt | ||||||||
| Sicherheitshinweise | ||||||||
| ||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||
L-Homocystein (Hcy) ist eine natürlich vorkommende (nicht proteinogene) α-Aminosäure. Sie ist im Stoffwechsel ein Zwischenprodukt des Ein-Kohlenstofftransfers und entsteht durch S-Demethylierung von L-Methionin als Methyldonor. Erhöhte Blutwerte für Homocystein können eine Schädigung der Blutgefäße zur Folge haben. Es steht auch in engem Zusammenhang mit Depressionen und Demenzerkrankungen im Alter. Normale Laborwerte bei der Blutuntersuchung liegen zwischen 5 und 10 µmol·l−1. Zur Regulierung des Homocysteinspiegels im Blut ist eine ausreichende Versorgung mit Betain und den Vitaminen B12, B6 sowie Folsäure erforderlich.[2] Eine Therapie mit den genannten Wirkstoffen zur Sekundärprophylaxe ist jedoch wissenschaftlich umstritten.
Zwei Moleküle Homocystein verbinden sich über eine Disulfidbrücke zum Homocystin. Bei erhöhtem Homocysteinspiegel im Blut wird Homocystin im Urin ausgeschieden (Homocystinurie).
Geschichte
Homocystein wurde 1932 von Vincent du Vigneaud bei seinen Arbeiten über schwefelhaltige Verbindungen entdeckt. Doch erst 1962 erkannten Carson und Neil den Zusammenhang zwischen Homocystein und bestimmten Erkrankungen. Sie fanden deutlich erhöhte Homocystinwerte im Urin einer Gruppe von Kindern mit geistiger Behinderung und postulierten einen Enzymdefekt – die klassische Homocystinurie, verursacht durch einen Defekt der Cystathionin-β-Transferase.[3][4][5]
Eigenschaften
Chemische Eigenschaften
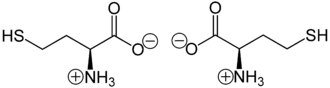
Homocystein liegt überwiegend als „inneres Salz“ bzw. Zwitterion vor, dessen Bildung dadurch zu erklären ist, dass das Proton der Carboxygruppe an das einsame Elektronenpaar des Stickstoffatoms der Aminogruppe wandert.
Zwitterionen von L-Homocystein (links) bzw. D-Homocystein (rechts)
Im elektrischen Feld wandert das Zwitterion nicht, da es als Ganzes ungeladen ist. Genaugenommen ist dies am isoelektrischen Punkt (bei einem bestimmten pH-Wert) der Fall, bei dem das Homocystein auch seine geringste Löslichkeit in Wasser hat. Durch seine im Vergleich zu Cystein zusätzliche CH2-Gruppe kann Homocystein einen fünfgliedrigen heterocyclischen Ring bilden, ein sogenanntes Thiolacton.[6] Diese Cyclisierungsreaktion verhindert die Bildung stabiler Peptidbindungen. Ein Protein, das Homocystein enthält, hat demnach die Tendenz, sich aufzuspalten.
Biochemische Bedeutung
Aus L-Homocystein und Methyl-FH4 kann durch das Enzym Methionin-Synthase die Aminosäure L-Methionin in einer Remethylierung gebildet werden. Die Methionin-Synthase benötigt Vitamin B12 als Coenzym. Alternativ kann Homocystein in Leber und Niere über die Betain-Homocystein-Methyltransferase zu Methionin umgewandelt werden. Coenzym für diese Reaktion ist Betain. Abgebaut wird Homocystein über die Transsulfurierung, einen rein Vitamin-B6-abhängigen Schritt.
L-Methionin wird einerseits zur Proteinsynthese, andererseits zur Bildung von S-Adenosylmethionin (SAM) biochemisch genutzt. SAM ist der wichtigste Donator für Methylgruppen im zellulären Stoffwechsel. Hat es seine Methylgruppe abgegeben, entsteht S-Adenosylhomocystein (SAH), das zu Adenosin sowie L-Homocystein hydrolysiert wird.

SAH hemmt Methylierungsreaktionen, sein Abbau zu Homocystein ist also zwingend notwendig, um Methylierungsreaktionen aufrechterhalten zu können. Ist der Abbau von Homocystein gestört, sind auch die wichtigen Methylierungsreaktionen in der Zelle gestört.[7]
Homocystein und Genetik
Genetischer Polymorphismus im Homocysteinstoffwechsel kann unter bestimmten Bedingungen die Enzymfunktion und somit auch den Homocysteinstoffwechsel beeinflussen. Meist führt eine Veränderung des genetischen Codes zu einer Verlangsamung im Abbau des Homocysteins und somit zu einem Anstieg der Homocysteinkonzentration im Blut. Klinisch relevante Polymorphismen sind vor allem im Enzym MTHFR (Methylentetrahydrofolat-Reduktase) zu finden.[8] Die häufigste vorkommende Mutation ist der Aminosäurenaustausch Alanin gegen Valin an der Position 677. Diese Form des Enzyms ist thermolabil und führt zu einer bis zu 50 % verminderten Leistung bei 37 °C (Körpertemperatur).
Homocystein und äußere Faktoren
Aufgrund äußerer Faktoren kann es zu einer milden bis moderaten Erhöhung der Homocysteinkonzentration im Blut kommen. Zu bedenken ist, dass eine Erhöhung des Homocysteinwertes in vielen Fällen ein multifaktorell ausgelöstes Phänomen ist. Erhöhte Homocysteinwerte findet man bei Alkoholkonsum,[9][10] Rauchen, häufigem Genuss von Kaffee, Bewegungsarmut und Übergewicht. Auch bestimmte Medikamente können die Homocysteinkonzentration beeinflussen. Ein Mangel an Folsäure und Cobalamin, der auch durch Entzündungsprozesse hervorgerufen werden kann,[11] führt ebenfalls zum Anstieg der Homocysteinwerte.[7]
Homocystein als Risikofaktor
Homocystein kann eine direkte toxische Schädigung der Gefäßwand hervorrufen und auf verschiedenen Wegen zu einer erhöhten Thromboseneigung führen. Patienten mit bekannter koronarer Herzkrankheit sind bereits bei leicht erhöhtem Homocysteinspiegel mit einem erhöhten Risiko für kardiovaskuläre Ereignisse belastet, während die Datenlage bei völlig gesunden Menschen uneinheitlich ist. Bei einem Homocysteinspiegel von über 15 µmol/l besteht einheitlich in mehreren Studien ein erhöhtes Risiko.
Obgleich Folsäure und B-Vitamine den Homocysteinspiegel nachweislich senken, haben sie in mehreren großen Studien bislang nicht zu einer Senkung des Risikos für Herzinfarkt, wohl aber zur Senkung des Schlaganfallrisikos (bis zu 25 % Reduktion)[12] geführt. Eine aktuelle (10/2009) Systematische Übersichtsarbeit der Cochrane Collaboration hat ergeben, dass die Supplementierung von B-Vitaminen für die Prävention von Herz-Krankheiten keine Rolle spielt.[13] Aus diesem Grunde wird die Bestimmung des Homocysteinspiegels meist nur für Patienten empfohlen, die keine anderen Risikofaktoren aufweisen. Eine Therapie wird bei Werten über 15 µmol/l überwiegend empfohlen.
Eine Studie mit Patienten, die an Multiple Sklerose erkrankt sind, hat ergeben, dass der Homocysteinspiegel mit dem Grad von Depression korreliert. Allerdings zeigte sich kein Zusammenhang mit deren Vitamin B12- und Folsäurewerten und dem Grad der Behinderung, was auf einen bisher unbekannten Faktor für den erhöhten Homocysteinspiegel schließen lässt.[14]
Kinder, die einen Schlaganfall erlitten haben, weisen signifikant häufiger eine Störung im Homocysteinstoffwechsel auf als Gesunde.[15] Bei Schwangeren korrelieren erhöhte Homocysteinkonzentrationen mit einem erhöhten Risiko einer Fehlgeburt sowie der Entwicklung von Schwangerschaftskomplikationen wie der Eklampsie.[16] Eine Erhöhung der Homocysteinwerte im Blut der Mutter ist ebenso ein Risikofaktor für die Entstehung von Neuralrohrdefekten beim Kind.[17]
Erhöhter Homocysteinspiegel ist ein Risikofaktor bei der Entstehung aller Stadien von Makuladegeneration.[18][19]Die Gabe eines Vitamin-B-Komplexes (Vitamin B6 - Pyridoxin, Vitamin B9 - Folsäure und Vitamin B12 - Cyancobalamin) senkt den Homocysteinspiegel, dies mindert signifikant (34 %) die Wahrscheinlichkeit eine Makuladegeneration zu entwickeln.[20]
Labordiagnostik
Die Bestimmung des Homocysteinspiegels im Blut erfolgt meist immunchemisch oder mittels HPLC. Als Material wird EDTA- oder Fluorid-Blut empfohlen. Da Homocystein von roten Blutkörperchen freigesetzt wird, kommt es ohne Zusatz von Hemmstoffen (Spezialröhrchen) zu einem Anstieg von ca. 10 % pro Stunde. Seit kurzem gibt es die Möglichkeit, den Homocysteinwert auch patientennah (Point-of-Care-Testing) zu messen. Damit wird es möglich, den Patienten noch während des Arztbesuches das Ergebnis der Untersuchung mitzuteilen bzw. eine eventuell notwendige Behandlung ohne Zeitverlust einzuleiten.
Die Kosten der Untersuchung von ca. 20 bis 30 € werden im Normalfall nicht von Krankenkassen übernommen und müssen vom Patienten als so genannte IGeL-Leistung selbst getragen werden.
Literatur
- Olaf Stanger: Homocystein: Grundlagen, Klinik, Therapie, Prävention. Maudrich, Wien/München/Bern 2004, ISBN 3-85175-766-1.
- Ger, Tymoczko, Stryer: Biochemie. 5. Auflage, Spektrum Akademischer Verlag, Heidelberg 2003, ISBN 3-8274-1303-6.
- Per Magne Ueland, Helga Refsum und Lars Brattström: 8. Plasma Homocysteine and Cardiovascular Disease. In: Robert Francis (Hrsg.): Atherosclerotic cardiovascular disease, hemostasis, and endothelial function. M. Dekker, New York 1992, ISBN 0-8247-8726-9, S. 183–236 (PDF 2,9 MB).
- Wolfgang Herrmann, Rima Obeid: Vitamins in the prevention of human diseases. 2011. ISBN 978-3-11-021448-2
- Wolfgang Herrmann, Rima Obeid: Die obligatorische Folsäurefortifikation von Nahrungsmitteln: Ein in Deutschland kontrovers diskutiertes Thema. The Mandatory Fortification of Staple Foods with Folic Acid: A Current Controversy in Germany. Ärzteblatt-Übersichtsarbeit, doi:10.3238/arztebl.2011.0249
Einzelnachweise
- ↑ 1,0 1,1 Günter Mayer, in: Römpp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ Vitamin-B12- und Folsäure-Spiegel niedrig, Risiko für Schlaganfälle erhöht.
- ↑ Gruson D.: Cardiovascular diseases and homocysteine, a short summary of a long story. J Int Clin Chem 2003;14:3. HTML (Version vom 27. Oktober 2007 im Internet Archive).
- ↑ du Vigneaud Vincent: A Trail of Sulfa Research: From Insulin to Oxytocin. Nob Lec 1955;1–10. PDF.
- ↑ CARSON NA, NEILL DW: Metabolic abnormalities detected in a survey of mentally backward individuals in Northern Ireland. In: Arch. Dis. Child.. 37, Oktober 1962, S. 505–513. doi:10.1136/adc.37.195.505. PMID 14018926. Volltext bei PMC: 2012909..
- ↑ H. S. Baernstein, Journal of Biological Chemistry 106 (1934) 451.
- ↑ 7,0 7,1 Durand P, Prost M, Loreau N.: Impaired homocysteine metabolism and atherothrombotic disease. Lab Invest 2001;81:645–72, PMID 11351038.
- ↑ Födinger M, Buchmayer H, Sunder-Plassmann G.: Molecular genetics of homocysteine metabolism. Miner Electrolyte Metab 1999;25:269–78, PMID 10681651.
- ↑ Bleich S, Bleich K, Kropp S, Bittermann HJ, Degner D, Sperling W, Rüther E, Kornhuber J. Moderate alcohol consumption in social drinkers raises plasma homocysteine levels: a contradiction to the "french paradox"? Alcohol Alcohol. 36:189-192, 2001. PMID 11373253
- ↑ Bleich S, Carl M, Bayerlein K, Reulbach U, Biermann T, Hillemacher T, Bönsch D, Kornhuber J. Evidence of increased homocysteine levels in alcoholism: the Franconian Alcoholism Research Studies (FARS). Alcohol.Clin.Exp.Res. 29:334-336, 2005. PMID 15770107
- ↑ Ploder M, Schroecksnadel K, Spittler A, Neurauter G, Roth E, Fuchs D. Moderate hyperhomocysteinemia in patients with multiple trauma and with sepsis predicts poor survival. Mol Med. 16:498-504, 2010.
- ↑ NEJM 354, 2006, S. 1567–1577.
- ↑ Martí-Carvajal A.J. et al: Homocysteine lowering interventions for preventing cardiovascular events; Cochrane Heart Group; 2009.
- ↑ Homocysteinspiegel bei Depression unter MS Patienten.
- ↑ van Beynum IM u. a.: Hyperhomocysteinaemia: a risk factor for ischemic stroke in children. In: Circulation 99, 1999, S. 2070–2072. PMID 10217643.
- ↑ Nelen WL: Hyperhomocysteinaemia and human reproduction. In: Clin Chem Lab Med 39, 2001, S. 758–763. PMID 11592447
- ↑ Fowler B: Disorders of homocysteine metabolism. In: J Inher Met Dis 20, 1997, S. 270–285, PMID 9211199.
- ↑ Plasma homocysteine, vitamin B12 and folate levels in age-related macular degeneration.Graefes Arch Clin Exp Ophthalmol 2006;244:565-569.
- ↑ C-reactive protein and homocysteine are associated with dietary and behavioral risk factors for age-related macular degeneration. Nutrition 2006;22:441-443.
- ↑ Folic Acid, Pyridoxine, and Cyanocobalamin Combination Treatment and Age-Related Macular Degeneration in Women. The Women’s Antioxidant and Folic Acid Cardiovascular Study. Arch Intern Med. 2009;169(4):335-341.
Weblinks
- Laborlexikon (ISSN 1860-966X) - Fachzeitschrift für Labormedizin: Homocystin
- Homepage der DACH-Liga Homocystein e.V.
- Homocystein: Vitamin-B-Prophylaxe in der Diskussion
- Homocysteine Expert Panel e.V.
- http://www.homocystein-forum.com
| Bitte den Hinweis zu Gesundheitsthemen beachten! |