Oleanolsäure
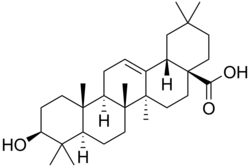
| Strukturformel | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||
| Allgemeines | |||||||||||||||
| Name | Oleanolsäure | ||||||||||||||
| Andere Namen |
| ||||||||||||||
| Summenformel | C30H48O3 | ||||||||||||||
| CAS-Nummer | 508-02-1 | ||||||||||||||
| PubChem | 10494 | ||||||||||||||
| Eigenschaften | |||||||||||||||
| Molare Masse | 456,71 g·mol−1 | ||||||||||||||
| Aggregatzustand |
kristalliner Feststoff | ||||||||||||||
| Schmelzpunkt | |||||||||||||||
| Löslichkeit |
unlöslich in Wasser, gut löslich in Methanol[1] | ||||||||||||||
| Sicherheitshinweise | |||||||||||||||
| |||||||||||||||
| LD50 | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||
Oleanolsäure ist ein pentazyklisches Triterpen, das aus fünf Cyclohexanringen aufgebaut ist. Das Saponin Oleanolsäure ist ein natürlicher Bestandteil einer Reihe von Pflanzen.
Vorkommen
Oleanolsäure ist als Naturstoff in einer Vielzahl von Pflanzen enthalten. Beispielsweise kann sie aus Salbei (Salvia officinalis), Gemeinem Efeu (Hedera helix),[4] Zuckerrüben (Beta vulgaris), Ginseng (Panax ginseng), Breitwegerich (Plantago major), Syzygium cumini, Pistazien (Pistazia vera), Olivenblättern (Olea europaea) und Weißbeerigen Misteln (Viscum album)[5] gewonnen werden.[6]
Pharmakologische Eigenschaften
Oleanolsäure ist schwach zytotoxisch und weist nur eine geringes anti-oxidatives Potenzial auf. Da die pharmakologisch interessanten Eigenschaften nur relativ schwach ausgeprägt sind, wurden verschiedene Derivate der Oleanolsäure hergestellt, die eine erheblich höhere Potenz haben.[7] Ein Derivat mit deutlich höherem Potenzial ist Bardoxolon (2-Cyan-3,12-dioxo-l,9-dien-28-oleanolsäure, CDDO), beziehungsweise dessen Methylester (Bardoxolon-Methyl). Bardoxolon ist eine vielversprechende chemopräventive und zytostatische Substanz, die anti-proliferativ und pro-apoptotisch wirkt.[8] Die Verbindung befindet sich in der klinischen Erprobung (Phase I/II).[9][10] Zur Behandlung von chronischer Niereninsuffizienz ist Bardoxolon-Methyl in der klinischen Phase III.[11]
Seit 1977 wird Oleanolsäure in China und Japan bei Lebererkrankungen als orales Therapeutikum verwendet. Seit 1986 gegen Hyperlipidämie und nichtlymphatische Leukämie. In Japan ist seit 1990 eine oleanolhaltige Creme zum Schutz vor Hautkrebs im Handel.[6]
Siehe auch
Weiterführende Literatur
- A. Bishayee, S. Ahmed, N. Brankov, M. Perloff: Triterpenoids as potential agents for the chemoprevention and therapy of breast cancer. In: Frontiers in bioscience Band 16, 2011, S. 980–996, ISSN 1093-4715. PMID 21196213. PMC 3057757. (Review).
- M. B. Sporn, K. T. Liby, M. M. Yore, L. Fu, J. M. Lopchuk, G. W. Gribble: New synthetic triterpenoids: potent agents for prevention and treatment of tissue injury caused by inflammatory and oxidative stress. In: Journal of natural products Band 74, Nummer 3, März 2011, S. 537–545, ISSN 1520-6025. doi:10.1021/np100826q. PMID 21309592. PMC 3064114. (Review).
- J. L. Ríos: Effects of triterpenes on the immune system. In: Journal of ethnopharmacology Band 128, Nummer 1, März 2010, S. 1–14, ISSN 1872-7573. doi:10.1016/j.jep.2009.12.045. PMID 20079412. (Review).
- I. Sogno, N. Vannini, G. Lorusso, R. Cammarota, D. M. Noonan, L. Generoso, M. B. Sporn, A. Albini: Anti-angiogenic activity of a novel class of chemopreventive compounds: oleanic acid terpenoids. In: Recent results in cancer research. Fortschritte der Krebsforschung. Progrès dans les recherches sur le cancer Band 181, 2009, S. 209–212, ISSN 0080-0015. PMID 19213570. (Review).
- A. Petronelli, G. Pannitteri, U. Testa: Triterpenoids as new promising anticancer drugs. In: Anti-cancer drugs Band 20, Nummer 10, November 2009, S. 880–892, ISSN 1473-5741. doi:10.1097/CAD.0b013e328330fd90. PMID 19745720. (Review).
- M. N. Laszczyk: Pentacyclic triterpenes of the lupane, oleanane and ursane group as tools in cancer therapy. In: Planta medica Band 75, Nummer 15, Dezember 2009, S. 1549–1560, ISSN 1439-0221. doi:10.1055/s-0029-1186102. PMID 19742422. (Review).
- B. Yu, J. Sun: Current synthesis of triterpene saponins. In: Chemistry, an Asian journal Band 4, Nummer 5, Mai 2009, S. 642–654, ISSN 1861-471X. doi:10.1002/asia.200800462. PMID 19294723. (Review).
- N. Sultana, A. Ata: Oleanolic acid and related derivatives as medicinally important compounds. In: Journal of enzyme inhibition and medicinal chemistry Band 23, Nummer 6, Dezember 2008, S. 739–756, ISSN 1475-6374. doi:10.1080/14756360701633187. PMID 18618318.
- J. Liu: Oleanolic acid and ursolic acid: research perspectives. In: Journal of ethnopharmacology Band 100, Nummer 1–2, August 2005, S. 92–94, ISSN 0378-8741. doi:10.1016/j.jep.2005.05.024. PMID 15994040. (Review).
- Z. Ovesná, A. Vachálková, K. Horváthová, D. Tóthová: Pentacyclic triterpenoic acids: new chemoprotective compounds. Minireview. In: Neoplasma Band 51, Nummer 5, 2004, S. 327–333, ISSN 0028-2685. PMID 15640935. (Review).
Einzelnachweise
- ↑ 1,0 1,1 T. Mühle: Trennung der Positionsisomere Oleanolsäure und Ursolsäure. Diplomica Verlag, 2009, ISBN 3-836-67870-5 S. 7 (eingeschränkte Vorschau in der Google Buchsuche).
- ↑ 2,0 2,1 2,2 2,3 Datenblatt Oleanolic acid bei Sigma-Aldrich, abgerufen am 24. April 2011.
- ↑ Seit 1. Dezember 2012 ist für Stoffe ausschließlich die GHS-Gefahrstoffkennzeichnung zulässig. Bis zum 1. Juni 2015 dürfen noch die R-Sätze dieses Stoffes für die Einstufung von Zubereitungen herangezogen werden, anschließend ist die EU-Gefahrstoffkennzeichnung von rein historischem Interesse.
- ↑ Salbei konzentriert – Wirkstoff der alten Heilpflanze effektiv gewinnen. Fachhochschule Münster, S. 26–27.
- ↑ S. Jäger, A. Scheffler, H. Schmellenkamp: Pharmakologie ausgewählter Terpene. In: Pharmazeutische Zeitung 22, 2006.
- ↑ 6,0 6,1 H. Schmandke: Triterpenoide in Oliven. In: Ernährungs Umschau 2, 2009, S. 92–95.
- ↑ A. Bishayee, S. Ahmed, N. Brankov, M. Perloff: Triterpenoids as potential agents for the chemoprevention and therapy of breast cancer. In: Frontiers in bioscience Band 16, 2011, S. 980–996, ISSN 1093-4715. PMID 21196213. PMC 3057757. (Review).
- ↑ D. Deeb, X. Gao, Y. Liu, D. Jiang, G. W. Divine, A. S. Arbab, S. A. Dulchavsky, S. C. Gautam: Synthetic triterpenoid CDDO prevents the progression and metastasis of prostate cancer in TRAMP mice by inhibiting survival signaling. In: Carcinogenesis Band 32, Nummer 5, Mai 2011, S. 757–764, ISSN 1460-2180. doi:10.1093/carcin/bgr030. PMID 21325633. PMC 3086702.
- ↑ Klinische Studie (Phase I/II): CDDO in Treating Patients With Metastatic or Unresectable Solid Tumors or Lymphoma bei Clinicaltrials.gov der NIH
- ↑ A. Petronelli, E. Pelosi, S. Santoro, E. Saulle, A. M. Cerio, G. Mariani, C. Labbaye, U. Testa: CDDO-Im is a stimulator of megakaryocytic differentiation. In: Leukemia research Band 35, Nummer 4, April 2011, S. 534–544, ISSN 1873-5835. doi:10.1016/j.leukres.2010.09.013. PMID 21035854.
- ↑ Klinische Studie (Phase III): Bardoxolone Methyl Evaluation in Patients With Chronic Kidney Disease and Type 2 Diabetes (BEACON) bei Clinicaltrials.gov der NIH
Weblinks
- Pharmakologie ausgewählter Terpene. Pharmazeutische Zeitung