Amalgam
Ein Amalgam (griechisch μαλακός malakos ‚weich‘ mit Alpha privativum, d. h. das „Nicht-Erweichende“; nach anderer Etymologie arab. al malagma ‚erweichende Salbe‘) ist in der Chemie eine Legierung des Quecksilbers. Als Amalgam im weiteren Sinne werden oft auch nicht (ohne weiteres) umkehrbare Vermischungen anderer Stoffe bezeichnet, meist die Legierung mehrerer Metalle. Im übertragenen Sinne werden als Amalgam auch Mischungen unterschiedlicher Begriffe, Ideen, Kulturen oder Traditionen bezeichnet.
Da viele Metalle in Quecksilber löslich sind (eine Ausnahme ist zum Beispiel Eisen), gibt es sehr viele Amalgame. Amalgame mit sehr großem Quecksilberanteil sind oft bei Raumtemperatur – wie das Quecksilber selbst – flüssig, bei kleineren Quecksilbergehalten sind sie fest.
In der klassischen Alchemie wird die Amalgamierung des Quecksilbers mit anderen Metallen oft mit der körperlichen Vereinigung verglichen. Als alchemistisches Lexem ist mlat. amalgama seit dem 13. Jahrhundert belegt.
Natürliche Amalgame

Es sind mehrere natürlich vorkommende Amalgame bekannt und von der IMA als eigenständige Minerale anerkannt[1]:
- Mit Blei: Bleiamalgam (Pb2Hg)
- Mit Kupfer: Belendorffit (Cu7Hg6), Kolymit (Cu7Hg6)
- Mit Palladium: Potarit (PdHg)
- Mit Silber: Eugenit (Ag11Hg2), Luanheit (Ag3Hg), Moschellandsbergit (Ag2Hg3), Paraschachnerit (Ag1,2Hg0,8), Schachnerit (Ag1,1Hg0,9)
- Mit Silber und Gold: Weishanit ((Au,Ag)3Hg2)
Technische Amalgame und ihre Verwendung
Zahnamalgam
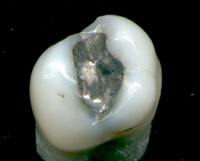
In der Zahnmedizin wird eine Legierung des Quecksilbers mit anderen Metallen, wie Silber, Kupfer, Indium, Zinn und Zink, in großem Umfang als Zahnfüllungsmaterial eingesetzt. Ein Zusammenhang mit ernsten Gesundheitsbeschwerden konnte nicht belegt werden. Eine Quecksilberbelastung ist jedoch minimal gegeben, ist jedoch im nicht messbaren Bereich.[2][3]
Natriumamalgam
Ein technisch wichtiges Reduktionsmittel in der organischen und anorganischen Chemie und in großem Maßstab hergestelltes Amalgam ist das Natriumamalgam, das bei der Chloralkali-Elektrolyse als Zwischenprodukt entsteht. Es wird mit Wasser zu Natronlauge, Wasserstoff und Quecksilber zersetzt, das im Kreislauf wieder zur Elektrolyse verwendet wird.
Ammoniumamalgam
Da die Alkalimetalle Amalgame bilden, zum Beispiel bei der Elektrolyse von Lösungen der Alkalimetallionen mit Quecksilberelektroden, hat man auch versucht, ein Ammonium- beziehungsweise Ammoniakamalgam herzustellen (das Ammoniumion verhält sich oft den Alkalimetallionen ähnlich); Ammoniumamalgam zersetzt sich aber zu Quecksilber, Ammoniak und Wasserstoff.
Goldamalgam
Bei der Goldgewinnung wird teilweise noch Quecksilber eingesetzt. Dieses bildet mit dem Gold, das in kleinen Flittern mit Gestein vermengt vorliegt, ein zunächst flüssiges Amalgam, das durch seine höhere Dichte von den leichteren Gesteinsresten abfließt. Um daraus reines Gold zu erhalten, wird das Amalgam erhitzt, um das Quecksilber auszudampfen; dieser Vorgang wird auch Abrauchen genannt. Dabei entstehen hochgiftige Quecksilberdämpfe.
Goldamalgame werden auch beim chemischen Vergolden, der sogenannten Feuervergoldung, verwendet. Dabei wird Goldamalgam auf einen metallischen Gegenstand aufgebracht oder aufgestrichen und durch Hitzeeinwirkung wird das Quecksilber verdampft.
Aluminiumamalgam
Aluminiumamalgam wird als Reduktionsmittel verwendet.
Thallium-Amalgam
Thallium-Amalgam wird wegen seines niedrigen Gefrierpunkts von -58 Grad Celsius als Thermometerflüssigkeit für Tieftemperaturthermometer verwendet.
Andere
Zinnamalgam bildete bis in die Mitte des 19. Jahrhunderts die reflektierende Beschichtung von Spiegeln.[4]
Amalgam kann als Ersatz für das ansonsten technisch notwendige flüssige Quecksilber in Energiesparlampen eingesetzt werden. Durch den Einsatz von Amalgam bleibt der Lichtstrom über einen größeren Temperaturbereich nahezu konstant. Dieser Vorteil wirkt sich vor allem beim Einsatz in geschlossenen Leuchten, Globe-Gehäusen und im Außenbereich aus. Ein Nachteil ist der geringe Anfangslichtstrom direkt nach dem Einschalten, da das Quecksilber erst bei höheren Temperaturen aus dem Amalgam verdampft.
Amalgamprobe

Quecksilbersalze sind im Unterschied zu Quecksilbermetall und Amalgam auf Grund ihrer Wasserlöslichkeit hochgiftig. Man weist sie durch die so genannte Amalgamprobe nach: Die salpetersaure Lösung wird auf ein Kupferblech gegeben – zurück bleibt ein nicht abwischbarer, silbriger Amalgamfleck:
- Redoxreaktion: Quecksilberkationen oxidieren Kupfer zu Kupferionen und Quecksilber.
Das Quecksilber bildet dabei mit dem Kupferblech eine Legierung, das Kupfer-Amalgam. Silbersalze würden ähnliche Flecken bilden; das dabei entstehende Silber ist jedoch abwischbar. Somit sind letztendlich Silbersalze von Quecksilbersalzen unterscheidbar.
Amalgamverfahren
Bei der Chloralkalielektrolyse zur großtechnischen Gewinnung von Chlor, Natronlauge und Wasserstoffgas wird bei dem Amalgamverfahren Quecksilber als Kathode eingesetzt, so dass sich das aus Salzwasser durch Reduktion bildende Natrium als Amalgam abscheidet. Anschließend wandert das Natriumamalgam zum Amalgamzersetzer, wo es mit Wasser zu salzfreier Natronlauge, Wasserstoffgas und Quecksilber reagiert. Dieses Elektrolyseverfahren hat den Vorteil, dass es kochsalzfreies Natriumhydroxid liefert (Natronlauge), ist jedoch ökologisch bedenklich, da den Produkten Quecksilberreste entzogen werden müssen (Nachreinigung, Entgiftung z. B. mit Aktivkohlefiltern).
Siehe auch
Weblinks
Einzelnachweise
- ↑ Mineralienatlas:Amalgam
- ↑ Pressemitteilung der LSRO zur Studie „LITTLE EVIDENCE TO LINK MERCURY FILLINGS TO HUMAN HEALTH PROBLEMS“
- ↑ Zahnfüllungen aus Amalgam sind ungefährlich Die Welt, 14. Dezember 2004
- ↑ Spiegelbau