Cyclodextrine
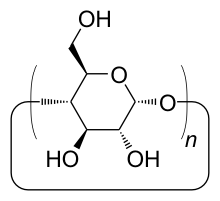
Cyclodextrine (CD) sind eine Klasse von Verbindungen, die zu den cyclischen Oligosacchariden gehören. Sie stellen ringförmige Abbauprodukte von Stärke dar. Sie bestehen aus α-1,4-glykosidisch verknüpften Glucosemolekülen. Dadurch entsteht eine toroidale Struktur mit einem zentralen Hohlraum. Cyclodextrine wurden erstmals von Villiers und Schardinger beschrieben, blieben aber lange Zeit eine Laborkuriosität. Sie wurden erstmals von Villiers 1891 isoliert und 1903 von Schardinger als Oligosaccharide charakterisiert.

Nomenklatur
Je nach Anzahl der sie aufbauenden Glucosemoleküle erhalten sie einen griechischen Buchstaben als Präfix:
- α-Cyclodextrin: n = 6 Glucosemoleküle (Hohlraumdurchmesser/-höhe: 4,7..5,3/7,9 Å)
- β-Cyclodextrin: n = 7 Glucosemoleküle (Hohlraumdurchmesser/-höhe: 6,0..6,5/7,9 Å)
- γ-Cyclodextrin: n = 8 Glucosemoleküle (Hohlraumdurchmesser/-höhe: 7,5..8,3/7,9 Å)
- δ-Cyclodextrin: n = 9 Glucosemoleküle
Über die oben erwähnten Cyclodextrine hinaus werden in der Fachliteratur Cyclodextrine mit wesentlich mehr Glucoseeinheiten detailliert beschrieben. Diese sind allerdings aufgrund der geringen Mengen und hohen Preise nicht von ökonomischer Bedeutung. Die weiteste technische Verbreitung haben β-Cyclodextrin und Hydroxypropyl-β-Cyclodextrin.
Gewinnung und Herstellung
Die Cyclodextrine werden im Allgemeinen aus Stärke gewonnen, die von speziellen Bakterien (zum Beispiel Bacillus macerans) enzymatisch abgebaut wird. Zum Einsatz kommt dabei vor allem Maisstärke – industriell interessant ist insbesondere die sortenreine Gewinnung von Cyclodextrinen, um die verschiedenen Hohlraumdurchmesser je nach einzuschließender Substanz auswählen zu können.
Eigenschaften
Allen niederen Cyclodextrinen eigen ist die hydrophobe Kavität im Innern und die polare Außenfläche. Dadurch sind die Cyclodextrine in der Lage, so genannte Einschlussverbindungen mit apolaren organischen Verbindungen zu bilden.
In alkalischen Lösungen sind Cyclodextrine sehr stabil, in sauren Lösungen (bei einem pH-Wert kleiner als 3) werden sie dagegen zersetzt. Sie haben keine festen Schmelzpunkte, sind aber bis etwa 200 °C stabil. Darüber beginnen sie sich zu zersetzen. Sie gelten als nicht toxisch und sind weitgehend stabil gegenüber menschlichen Verdauungsenzymen.
Verwendung
Die Fähigkeit zu Einschlussverbindungen mit apolaren organischen Verbindungen und die Wasserlöslichkeit machen Cyclodextrine zu einem immer wichtigeren Gegenstand der pharmazeutischen Forschung, da die Komplexe mit Pharmazeutika in der Regel besser wasserlöslich sind als die reinen Pharmazeutika und daher auch im Körper leichter verfügbar sind. Weiterhin ist ihre Fähigkeit, die eingeschlossene Substanz vor umgebenden Verbindungen (zum Beispiel Sauerstoff) zu schützen sowie die eingeschlossenen Substanzen über einen längeren Zeitraum abzugeben, von großem Interesse.
α-Cyclodextrin ist seit 2008 in der Europäischen Union als lösliche Nahrungsfaser zugelassen.[1] Aufgrund seiner komplexbildenden Eigenschaften findet es Einsatz als Emulgator in der Lebensmittel- (Mayonnaisen) und Kosmetikindustrie (Hautcremes). Beta-Cyclodextrin ist in der EU als Lebensmittelzusatzstoff der Nummer E 459 mit unterschiedlichen Höchstmengenbeschränkungen für bestimmte Lebensmittel zugelassen, im Einzelnen bei der Aromatisierung von Tees oder Instant-Getränkepulvern (mit 0,5 Milligramm pro Kilogramm in der vorgesehenen Verzehrzubereitung) und Knabbererzeugnissen (mit 1 Milligramm pro Kilogramm) sowie bei tablettierten Lebensmitteln (nach Bedarf – quantum satis).[2] Gamma-Cyclodextrin wurde von der EU für die Wacker Chemie AG als neuartige Lebensmittelzutat für Nahrungsmittel- und Getränkeanwendungen zugelassen.[3]
Darüber hinaus begegnen dem Verbraucher Cyclodextrine unter dem Handelsnamen Febreze, Bounce oder Oust. Die in diesen Produkten befindlichen Cyclodextrinderivate binden die für unangenehme Gerüche verantwortlichen Verbindungen und sind gleichermaßen Träger von Duftstoffen. In manchen Ländern (zum Beispiel USA, Japan) sind Cyclodextrine als Lebensmittelzusatzstoffe zugelassen, da sie unter anderem den Geschmack und Geruch der eingeschlossenen Substanzen aufheben oder wieder freigeben können. Das Einsatzspektrum von Cyclodextrinen umfasst heute von verschiedenen Medikamentenzubereitungen über Pappkartons bis hin zur Medizin, Landwirtschaft und Sensorik diverse Einsatzbereiche. Das deutsche Textilforschungsinstitut in Krefeld erforscht intensiv die Nutzung von kovalent an die Stofffasern gebundenen Cyclodextrinen für „intelligente“ Textilien. Diese können sowohl über die Haut aufzunehmende Medikamente enthalten als auch Schweißgeruch binden.
Cyclodextrine können auch in Alkoholpulver verwendet werden. [4]
In der analytischen Chemie und mit besonders großem Erfolg in der Gaschromatographie werden spezielle Cyclodextrinderivate eingesetzt, um Gemische von Enantiomeren zu trennen. Ebenso erfolgreich sind Cyclodextrinderivate in der Kapillarelektrophorese (englisch CE) etabliert. Mit sulfatierten, geladenen Cyclodextrinen wird dadurch sogar eine Trennung von neutralen Enantiomeren möglich, die mittels CE ansonsten nicht zugänglich wären.[5]
Literatur
- Villiers A., Sur la transformation de la fécule en drextrine par le ferment butyrique, Compt. Rend. Fr. Acad. Sci. 1891:435-8
- Biwer A, Antranikian G, Heinzle E. Enzymatic production of cyclodextrins. Appl Microbiol Biotechnol 2002;59:609-17. PMID 12226716.
Einzelnachweise
- ↑ Genehmigung des Inverkehrbringens von alpha-Cyclodextrin als neuartige Lebensmittelzutat (2008/413/EG)
- ↑ Begrenzt zugelassene Zusatzstoffe, Anlage 4 (zu § 5 Absatz 1 und § 7) der Zusatzstoff-Zulassungsverordnung vom 29. Januar 1998 (Bundesgesetzblatt I, Seiten 230, 231), die zuletzt durch Artikel 1 der Verordnung vom 28. März 2011 (Bundesgesetzblatt I, Seite 530) geändert worden ist
- ↑ WACKER erhält Zulassung von gamma-Cyclodextrin als neue Lebensmittelzutat für Nahrungsmittel und Getränke in der EU. Presseinformation Wacker Chemie AG, 28. Juni 2012
- ↑ Brausepulver: Alkopops aus der Tüte, Westdeutsche Zeitung vom 28. Oktober 2004 (online abgerufen am 22. Juni 2007, am 4. April 2011 nicht mehr im Netz.)
- ↑ C. Bicchi; Cyclodextrin derivatives as chiral selectors for direct gas chromatographic separation of enantiomers in the essential oil, aroma and flavour fields in Journal of Chromatography A 1999, 843, 99–121; online abgerufen am 1. Januar 2013
Weblinks
- Ausführliche Übersicht über Cyclodextrine (PDF, 1,52 MB)
- CTD, Inc, Cyclodextrin Resource (englisch)