Acetylformoin
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
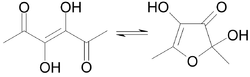
| |||||||
| Allgemeines | |||||||
| Name | Acetylformoin | ||||||
| Andere Namen |
| ||||||
| Summenformel | C6H8O4 | ||||||
| CAS-Nummer | 10153-61-4 | ||||||
| Kurzbeschreibung |
Intensiv karamellartig riechender[1] Feststoff mit bitterem Geschmack[2] | ||||||
| Eigenschaften | |||||||
| Molare Masse | 144,13 g·mol−1 | ||||||
| Aggregatzustand |
fest | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Acetylformoin ist ein sehr reaktives Abbauprodukt von Kohlenhydraten (Hexosen) wie der Glucose. Die Substanz ist ein Diketo-Endiol mit sechs Kohlenstoffatomen, die z. B. bei der Maillard-Reaktion als Zwischenprodukt entsteht und intensiv nach Karamell riecht.
Darstellung
Die Prozesse bei der Maillard-Reaktion sind sehr komplex und führen bei genügend hohen Temperaturen zu Melanoidinen, wobei Acetylformoin als reaktive Zwischenstufe gebildet wird.[4] Formal entsteht das Acetylformoin unter Abspaltung zweier Wassermoleküle aus Glucose über sogenannte Desoxyosone:[5]
Bei der Reaktion von Disacchariden entstehen strukturell sehr ähnliche, substituierte Derivate des Acetylformoins.[4]
Eigenschaften
Acetylformoin kann sowohl in einer offenkettigen Form, als auch wie die Kohlenhydrate in einer cyclischen „Furenose“-Halbacetal-Form vorkommen. Die Verbindung ist sehr reaktiv und bildet bei der weiteren Maillard-Reaktion mit Aminosäuren oder Proteinen Melanoidine wie das Pronyl-Lysin. Allgemeiner entstehen Aminohexosereduktone bzw. Glycosylamine.[4] Acetylformoin selbst besitzt einen bitteren Geschmack.[2] Die offenkettige Form riecht intensiv nach Karamell, wohingegen die cyclische Ketalform geruchlos ist. In protischen Lösungsmitteln wie Wasser wird sofort die ringförmige, nicht riechende Form gebildet.[1][6]
Siehe auch
Einzelnachweise
- ↑ 1,0 1,1 Wolfgang Engel : Geruchsaktive Verbindungen aus der Maillard-Reaktion schwefelfreier sowie schwefelhaltiger Aminkomponenten mit Fructose, Deutsche Forschungsanstalt für Lebensmittelchemie, 1999.
- ↑ 2,0 2,1 Kirsten Zeiter: Neue Methoden zur Synthese konformativ eingeschränkter Peptidmimetika, 11. September 2001, Ludwig-Maximilians-Universität München.
- ↑ Diese Substanz wurde in Bezug auf ihre Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ 4,0 4,1 4,2 Anke Hollnagel: Beiträge zur Chemie der nichtenzymatischen Bräunung von oligomeren Kohlenhydraten, TU Berlin, 19. April 2000.
- ↑ Ingrid Steiner: Vorlesung Lebensmittelchemie und Technologie, TU Wien.
- ↑ Deutsche Forschungsanstalt für Lebensmittelchemie: Jahresbericht, 2001.
