Anomerer Effekt
In der organischen Chemie bezeichnet der anomere Effekt die Tendenz eines Heteroatoms, welches an ein Kohlenstoffatom neben einem Heteroatom im Cyclohexanring substituiert ist, die axiale Position gegenüber der (sterisch weniger gehinderten!) äquatorialen Position vorzuziehen, was sterischen Betrachtungen widerspricht. Anders ausgedrückt ist bei Vorliegen zweier elektronegativer Substituenten an einem Kohlenstoffatom die synclinale Anordnung zweier Bindungen gegenüber der antiperiplanaren bevorzugt. Das Kohlenstoffatom, an das die betreffenden Substituenten gebunden sind, wird als anomerer Kohlenstoff bezeichnet. Im Formelschema ist die Bildung von Molekül 2 mit synclinaler Anordnung der rot markierten Bindungen gegenüber 1 bevorzugt.
Dieser stereoelektronische Effekt tritt auch für jedes der gezeigten Moleküle einzeln auf, da sie in ihrer Sesselkonformation invertieren können. Eine axial stehende Hydroxyfunktion wird damit in eine äquatoriale überführt und umgekehrt; auch hierbei ist diejenige Konformation, in der die OH-Gruppe axial steht, in beiden Fällen bevorzugt.
Der anomere Effekt wurde zuerst in Pyranen beobachtet.
Für die Erklärung dieses Effekts gibt es zwei Ansätze. Die einfachere Erklärung basiert auf der klassischen Physik. In der äquatorialen Konformation sind die Dipole beider Heteroatome in einer Ebene, und stoßen sich so mehr ab. Die komplexere Erklärung basiert auf der Quantenmechanik und ist weitgehend anerkannt. Zwischen dem freien Elektronenpaar des Heteroatoms und dem σ*-Orbital der C-X-Bindung findet negative Hyperkonjugation statt, was energetisch günstig ist. Dies ist in der folgenden Darstellung veranschaulicht, wobei die Atombezeichnungen für die Sauerstoffatome sowie das zweite freie Elektronenpaar des hinteren Sauerstoffatoms aus Gründen der Übersichtlichkeit ausgeblendet sind.
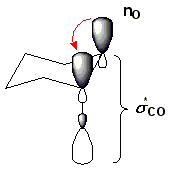
Literatur
- Hans Beyer, Wolfgang Walter: Lehrbuch der organischen Chemie, S. Hirzel Verlag, Stuttgart, 19. Auflage, ISBN 3-7776-0356-2.
- P. Collins, R. Ferrier: Monosacharides - Their Chemistry and their Roles in Natural Products, Wiley West Sussex 1995, ISBN 0-471-95343-1.